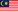SESI LIBAT URUS MDA BERSAMA INDUSTRI PERANTI PERUBATAN: MESYUARAT PRE-COUNCIL APEC CONSENSUS FRAMEWORK & MESYUARAT MICC BIL. 1/2025 KE ARAH MEMPERKUKUH KERJASAMA STRATEGIK
SESI LIBAT URUS MDA BERSAMA INDUSTRI PERANTI PERUBATAN: MESYUARAT PRE-COUNCIL APEC CONSENSUS FRAMEWORK & MESYUARAT MICC BIL. 1/2025 KE ARAH MEMPERKUKUH KERJASAMA STRATEGIK

Pada 8 Julai 2025, Pihak Berkuasa Peranti Perubatan (MDA) telah menganjurkan sesi libat urus yang merangkumi dua perbincangan utama bersama wakil-wakil industri serta persatuan berkaitantermasuk Association of Malaysian Medical Industries (AMMI), Malaysia Medical Device Association (MMDA), Malaysian Rubber Glove Manufacturers Association (MARGMA), Persatuan Pengilang-Pengilang Peranti Perubatan Malaysia (PERANTIM) dan Malaysia Dental Industry Association (MDIA). Sesi ini bertujuan memperkukuh kerjasama strategik serta menyelaras hala tuju kawal selia sektor peranti perubatan negara.
Sesi 1: Mesyuarat Pre-Council APEC Consensus Framework
Sesi pertama iaitu Pre-Council APEC Consensus Framework memberi tumpuan kepada pembentangan awal cadangan kepada industri peranti perubatan berkenaan Malaysia Consensus Framework for Ethical Collaboration in the Healthcare Sector, yang dirancang sebagai satu inisiatif nasional untuk memperkukuh tadbir urus dan budaya etika dalam sektor kesihatan, termasuk industri peranti perubatan.
Cadangan ini selaras dengan hala tuju yang digariskan dalam Business Ethics for APEC SMEs Initiative: Vision 2025, iaitu pelan tindakan lima tahun APEC yang dilancarkan pasca pandemik COVID-19 bagi menyokong pembangunan sistem kesihatan yang lebih beretika, inklusif dan berdaya tahan. Vision 2025 menggalakkan pelaksanaan prinsip etika perniagaan secara sukarela, khususnya melalui penerapan Kuala Lumpur Principles for Medical Device Sector Codes of Ethics.
Prinsip ini menekankan kepentingan penglibatan empat kumpulan utama iaitu industri, pengamal kesihatan, organisasi pesakit, dan kerajaan dalam membentuk budaya integriti, ketelusan dan tadbir urus beretika dalam sektor peranti perubatan.
Sehubungan itu, sesi ini telah menjadi medan awal bagi MDA mendapatkan maklum balas langsung daripada wakil industri peranti perubatan, khususnya bagi memastikan rangka kerja ini dapat direalisasikan secara berkesan, diterima industri, dan diselaraskan dengan dasar negara.
Sesi 2: Mesyuarat MDA–Industry Collaborative Committee (MICC) Bil. 1/2025
Sesi seterusnya, Ketua Eksekutif MDA telah mempengerusikan Mesyuarat MDA–Industry Collaborative Committee (MICC) Bil. 1/2025 yang membincangkan agenda berikut:
- Isu-isu yang dibangkitkan oleh pihak industri, dengan perbincangan tertumpu kepada maklum balas terhadap isu-isu tersebut dan langkah-langkah penambahbaikan untuk membantu industri memahami serta mematuhi kehendak kawal selia. Ini termasuk perkara berkaitan proses penilaian pematuhan, pelaksanaan sistem e-Permit, pengurusan maklumat melalui sistem atas talian, keperluan kepada penambahbaikan dokumen panduan teknikal.
- MDA turut membentangkan regulatory updates berkenaan perkembangan kawal selia merangkumi:
- Polisi baharu berkaitan Designated Medical Devices (DMD), Orphaned/Obsolete/Discontinued Devices (OOD), Innovative Devices, dan pelaksanaan Unique Device Identifier (UDI), eLabelling & eIFU, struktur fi baharu bagi pendaftaran peranti Kelas A, serta penguatkuasaan terhadap pengedar mengikut Akta 737;
- Kemajuan pembangunan sistem MEDCAST 3.0;
- Pembangunan Change Management untuk peranti yang telah berdaftar;
- Aktiviti pasca-pasaran termasuk pemantauan penjualan dalam talian, prosedur pengendalian aduan melibatkan fasiliti kesihatan dan pengguna;
- Aktiviti penguatkuasaan yang telah dijalankan;
- Program pembangunan industri, merangkumi Program Keusahawanan dalam Sektor peranti perubatan, Lawatan Kerja Regulatori dan Projek Pembangunan Di Bawah Rancangan Malaysia Ke-13 (RMK13)
- Perkembangan inisiatif serantau dan antarabangsa: Medical Device Regulatory Reliance Activity;
- Persediaan MDA ke arah penarafan WHO Global Benchmarking Tool (GBT); dan
- Penganjuran International Medical Device Exhibition and Conference (IMDEC) 2026.
MDA amat menghargai komitmen, kerjasama dan pandangan konstruktif daripada semua pihak industri. Mesyuarat seperti ini penting dalam memastikan dasar dan sistem kawal selia negara terus bersifat responsif, progresif, dan selari dengan keperluan industri serta kepentingan awam.

Disediakan oleh : Bahagian Hubungan Antarabangsa dan Industri (BHAI)
Dimuatnaik oleh : Bahagian Komunikasi Korporat
Tarikh muatnaik : 11 Julai 2025